Živa(I) nitrat
| Živa(I) nitrat[1][2] | |||
|---|---|---|---|
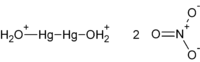 | |||
| IUPAC ime |
| ||
| Drugi nazivi | Živin nitrat | ||
| Identifikacija | |||
| CAS registarski broj | 10415-75-5  Y, (anhidrid) Y, (anhidrid)[7782-86-7] (dihidrat) | ||
| PubChem[3][4] | 11318980 | ||
| ChemSpider[5] | 9493944  Y Y | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | Hg2(NO3)2 (anhydrous) Hg2(NO3)2·2H2O (dihydrate) | ||
| Molarna masa | 525,19 g/mol (anhidrat) 561,22 g/mol (dihidrat) | ||
| Agregatno stanje | Beli kristali (anhidrat) bezvojni kristali (dihidrat) | ||
| Gustina | ? g/cm3 (anhidrat) 4,8 g/cm3 (dihidrat) | ||
| Tačka topljenja | ? (anhidrat) | ||
| Rastvorljivost u vodi | neznatno rastvoran, reaktivan | ||
| Opasnost | |||
| NFPA 704 |  1 3 1 OX | ||
| Srodna jedinjenja | |||
| Drugi anjoni | Živa(I) fluorid Živa(I) hlorid Živa(I) bromid Živa(I) jodid | ||
| Drugi katjoni | Živa(II) nitrat | ||
| Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
Živa(I) nitrat je hemijsko jedinjenje sa formulom HgNO2. Ono se koristi u pripremi drugih živa(I) jedinjenja, i poput drugih živinih jedinjenje je toksično.
Reakcije
Živa(I) nitrat se formira kombinovanjem žive sa razblaženom azotnom kiselinom (koncentrovana azotna kiselina bi proizvela živa(II) nitrat). Živa(I) nitrat je redukujući agens koji se oksiduje u kontaktu sa vazduhom.
Rastvori živa(I) nitrata su kiseli usled spore reakcije sa vodom:
- Hg2(NO3)2 + H2O → Hg2(NO3)(OH) + HNO3
Hg2(NO3)(OH) formira žuti talog.
Ako se rastvor zagreje do ključanja ili izloži svetlosti, živa(I) nitrat podleže reakciji disproporcionacije proizvodeći elementarnu živu i živa(II) nitrat[2]:
- 2Hg2(NO3)2 → Hg + Hg(NO3)2
Reference
- ↑ Lide, David R. (1998), Handbook of Chemistry and Physics (87 izd.), Boca Raton, FL: CRC Press, pp. 4-45, ISBN 978-0-8493-0594-8
- ↑ 2,0 2,1 Patnaik, Pradyot (2003), Handbook of Inorganic Chemical Compounds, McGraw-Hill Professional, pp. 573, ISBN 978-0-07-049439-8, pristupljeno 20. 7. 2009
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519. edit
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846. edit
Spoljašnje veze
 | Portal Hemija |









