Picolina
| Picolina | |||
| Nome | 2-Picolina | 3-Picolina | 4-Picolina |
| Outros nomes | α-Picolina, 2-Metilpiridina | β-Picolina, 3-Metilpiridina | γ-Picolina, 4-Metilpiridina |
| Fórmula estrutural |  |  |  |
| Número CAS | 109-06-8 | 108-99-6 | 108-89-4 |
| 1333-41-1 (Mistura de isômeros) | |||
| PubChem | 7975 | 7970 | 7963 |
| Fórmula molecular | C6H7N | ||
| Massa molar | 93,13 g·mol−1 | ||
| Estado físico | líquido | ||
| Apresentação | líquido incolor | ||
| Ponto de fusão | −69,9 °C[1] | −18 °C[2] | 3 °C[3] |
| Ponto de ebulição | 128 °C[1] | 144 °C[2] | 145 °C[3] |
| pKs[4] (o ácido conjugado BH+) | 5,94 | 5,63 | 6,03 |
| Solubilidade | completamente miscível com água | ||
| Identificação GHS |   Atenção[1] |   Perigo[2] |   Perigo[3] |
| Frases H e P | 226‐302‐312‐332‐319‐335 | 226‐302+332‐311‐315‐319‐335 | 226‐311‐332‐302‐319‐335‐315 |
| veja acima | veja acima | veja acima | |
| 210‐302+352‐305+351+338 | 10‐280‐302+352‐304+340 305+351+338‐309+310 | 280‐302+352‐304+340 305+351+338‐309+310 | |
| Informações de perigo [1][2][3] |  Substância nociva (Xn) |  Substância nociva (Xn) |  Veneno (T) |
| Frases R | 10‐20/21/22‐36/37 | 10‐20/21/22‐36/37/38 | 10‐20/22‐24‐36/37/38 |
| Frases S | (2) - 26 - 36 | 26 - 36/37 | (1/2) - 26 - 36/37 -45 |
Os compostos orgânicos picolinas, ou metilpiridinas, formam em Química uma família de compostos, pertencente aos compostos heterocíclicos (mais precisamente: heteroaromáticos). Consistem de um anel piridina, substituído com um grupo metila. Através de arranjo diferente resultando em três isômeros constitucionais com a fórmula C6H7N. São bastante semelhantes em suas propriedades em relação a piridina, e em aplicações que não dependem da estrutura molecular substituí-la facilmente como solventes. Caso contrário, elas são, em muitos aspectos, blocos de construção sintéticos para a fabricação de produtos farmacêuticos, agroquímicos e corantes.[5]
História
A 2-picolina foi isolada pela primeira vez em 1846 por Thomas Anderson do alcatrão de hulha.[6] O termo picolina consiste no latinismo pix (betume) e oleum (óleo) em conjunto.[5]
Obtenção
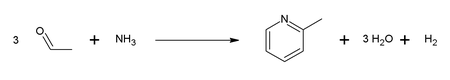
Atualmente, a 2-picolina é obtida principalmente por meio de duas rotas sintéticas: por condensação de acetaldeído, formol e amônia [7] e por ciclização de nitritos e acetileno (ciclização de Bönnemann).[8] Um exemplo é a reação de acetaldeído e amônia:
Aproximadamente 8000 t foram produzidas em todo o mundo em 1989.[7]
A 3-metilpiridina é preparada industrialmente por meio da reação de acroleína com amônia:[7]
Uma maneira mais eficiente é baseado em acroleína, propionaldeído e amônia:
Aproximadamente 9000 t foram produzidas em todo o mundo em 1989.[9]
Propriedades
As picolinas são líquidos incolores com um cheiro similar ao da piridina. São miscíveis com água, etanol e éter dietílico.[5] A 4-picolina, que tem simetria a mais elevada, apresenta o ponto de fusão mais alto.
Uma vez que os grupos metilo na posição 2 e 4 das respectivos isômeros de picolina estão dispostos em conjugação direta com o átomo de nitrogênio na remoção de elétrons, os grupos metilo nestes dois isômeros podem ser relativamente facilmente deprotonados por bases fortes, tais como di-isopropilamida de lítio ou butil-lítio e, em seguida, ainda obtendo-se derivados.[10]
Usos
Picolinas são utilizadas como intermediários para a preparação de outros compostos químicos. Por exemplo, a 2-vinilpiridina e o agroquímico nitrapirina podem ser preparados a partir da 2-picolina.[7] A 3-picolina é usada como material de partida para a síntese do insecticida clorpirifós e da vitamina niacina (vitamina B3),[7] a 4-picolina para a produção do fármaco anti-tuberculose isoniazida.[7]
Por oxidação, por exemplo, por permanganato de potássio (KMnO4),[7][11] resultando no ácido picolínico a partir de 2-picolina, em ácido nicotínico da 3-picolina e no ácido isonicotínico da 4-picolina.
Ver também
Referências
- ↑ a b c d Registo de 2-Methylpyridin na Base de Dados de Substâncias GESTIS do IFA.
- ↑ a b c d Registo de 3-Methylpyridin na Base de Dados de Substâncias GESTIS do IFA.
- ↑ a b c d Registo de 4-Methylpyridin na Base de Dados de Substâncias GESTIS do IFA.
- ↑ CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- ↑ a b c Methylpyridine - Römpp Lexikon Chemie
- ↑ T. Anderson: „On the constitution and properties of Picoline, a new organic base from Coal Tar“; in: Edinburgh New Phil. J.; 1846; XLI; S. 146–156 und 291–300 (http://books.google.com.br/books?id=lB0AAAAAMAAJ&pg=PA146&f=false).
- ↑ a b c d e f g Shinkichi Shimizu, Nanao Watanabe, Toshiaki Kataoka, Takayuki Shoji, Nobuyuki Abe, Sinji Morishita, Hisao Ichimura: „Pyridine and Pyridine Derivatives“, Ullmann's Encyclopedia of Industrial Chemistry, 2002 (doi:10.1002/14356007.a22_399).
- ↑ A. Behr: Angewandte homogene Katalyse, Wiley-VCH, Weinheim 2008, ISBN 3-527-31666-3, S. 722.
- ↑ Eric F. V. Scriven, Ramiah Murugan: „Pyridine and Pyridine Derivatives“, Kirk-Othmer Encyclopedia of Chemical Technology, 2005; XLI (doi:10.1002/0471238961.1625180919031809.a01.pub2).
- ↑ M. Sainsbury, M. Berry, J. D. Hepworth, C. Drayton, E. W. Abel, D Phillips, J. D. Woollins, A. G. Davies: Heterocyclic Chemistry, 1. Auflage, Royal Society of Chemistry, 2009, ISBN 0-85404-652-6, S. 30.
- ↑ Harold Hart (Autor), Leslie E. Craine (Autor), David J. Hart (Autor), Christopher M. Hadad (Autor); Nicole Kindler (Übersetzer): Organische Chemie, 3. Auflage, Wiley-VCH, Weinheim 2007, ISBN 978-3-527-31801-8, S. 494.