Ácido butanoico
| Ácido butanoico Alerta sobre risco à saúde | |
|---|---|
 | |
 | |
 | |
 | |
| Nome IUPAC | Ácido butanoico |
| Outros nomes | Ácido butírico |
| Identificadores | |
| Número CAS | 107-92-6 |
| PubChem | 264 |
| ChemSpider | 259 |
| MeSH | Butyric+acid |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | C4H8O2 |
| Massa molar | 88.1051 g/mol |
| Aparência | Oleoso, incolor |
| Densidade | 0,96 g·cm-3 (20 °C)[1] |
| Ponto de fusão | -5 °C[1] |
| Ponto de ebulição | 163 °C[1] |
| Solubilidade em água | miscível[2] |
| Solubilidade | miscível com etanol e éter dietílico[2] methanol 10.94 M[3] |
| Pressão de vapor | 0,9 hPa (20 °C)[1] |
| Acidez (pKa) | 4,82[4] |
| Riscos associados | |
| Principais riscos associados | Corrosive; Harmful to aquatic organisms |
| Frases R | R34 |
| Frases S | S1/2 S26 S36 S45 |
| Ponto de fulgor | 72 °C |
| Temperatura de auto-ignição | 452 °C |
| Número RTECS | ES5425000 |
| Compostos relacionados | |
| Outros aniões/ânions | Butiramida Cloreto de butirila |
| Outros catiões/cátions | Butiratos |
| Ácidos carboxílicos relacionados | Ácido propanoico (C3) Ácido valérico (C5) Ácido caproico (C6) Ácido isobutanoico Ácido succínico (butanodioico) Ácido alfa-hidroxibutírico |
| Compostos relacionados | Butanol Butanal Butanoato de metila Butanoato de etila |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
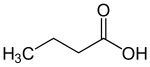
O ácido butanoico (ou ácido butírico) é um ácido monocarboxílico, saturado, de cadeia aberta, com fórmula molecular C4H8O2, massa molecular 88 u, e de fórmula estrutural CH3-CH2-CH2-COOH.
O nome usual ácido butírico é de origem grega: βουτυρος que significa "manteiga".
É o componente orgânico encontrado na manteiga rançosa, sendo um dos responsáveis pelo seu odor e sabor peculiares. É formado após a ação de micro-organismos sobre moléculas de gordura (triglicerídeos) presentes na manteiga.
Está presente tanto em alguns queijos, quanto no vômito, o que caracteriza o odor azedo dos dois.
Obtenção
Comercialmente é obtido a partir da oxidação do n-butiraldeído, derivado do acetileno, em presença de catalisadores:
- Acetileno → aldeído acético → crotonaldeído + H2 → n-butiraldeído + Ar (catalisador) → Ácido butírico
Equações:
- 2 C2H2 → 2 CH3-COH → CH3-CH=CH-COH + H2 → CH3-CH2-CH2-COH + ar → CH3-CH2-CH2-COOH
Aplicações e usos
- Ésteres do ácido butírico são produzidos para serem usados como sabores artificiais.
- Ésteres obtidos a partir da reação do ácido butírico com glicol ou glicerina são usados como agentes plastificantes.
- Os seus sais de cálcio são usados no tratamento do couro.
Referências
- ↑ a b c d Registo de CAS RN 107-92-6 na Base de Dados de Substâncias GESTIS do IFA, accessado em 06.01.2008.
- ↑ a b Thieme Chemistry, ed. (2009). RÖMPP Online - Version 3.5. Stuttgart: Georg Thieme Verlag KG
- ↑ «Solubility of butyric acid in methanol» [ligação inativa]
- ↑ Peter W. Atkins, Julio de Paula: Physikalische Chemie, 4. Auflage, Wiley-VCH, Weinheim 2006, S. 1118, ISBN 978-3-527-31546-8.
Bibliografia
- Voet & Voet; John Wiley & Sons, 1995
 | Este artigo sobre um composto orgânico é um esboço. Você pode ajudar a Wikipédia expandindo-o. |
 Portal da ciência
Portal da ciência Portal da química
Portal da química













