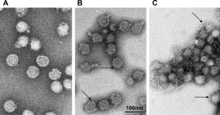
Virus della encefalite trasmessa da zecche
 | |
|---|---|
 | |
| Classificazione scientifica | |
| Dominio | Riboviria |
| Regno | Orthornavirae |
| Phylum | Kitrinoviricota |
| Classe | Flasuviricetes |
| Ordine | Amarilloviricetes |
| Famiglia | Flaviviridae |
| Genere | Flavivirus |
| Specie | Tick-borne encephalitis virus |
I virus della encefalite trasmessa da zecche (Tick-borne encephalitis virus, TBEV) sono una specie di arbovirus della famiglia Flaviviridae, genere Flavivirus, appartiene al IV gruppo dei virus a ((+) ssRNA). Esso è associato alla encefalite virale trasmessa dalle zecche.
Il virus fa parte dei flavivirus patogeni per l'uomo.[1]
Virologia
Questo virus ha un genoma a singolo filamento di RNA positivo ((ss) (+) RNA], esso può essere distinto in tre sottotipi:[2]
- Sottotipo dell'Estremo Oriente: Presente principalmente in Russia ad est degli Urali e in alcune parti della Cina, Giappone e Corea, portatori di questo sottotipo è Ixodes persulcatus, la letalità di questo sottotipo arriva fino al 20%.
- Sottotipo occidentale: Presente in Europa centrale, orientale e Nord Europa, vettore è Ixodes ricinus, la letalità arriva fino al 2%
- Sottotipo Siberiano Presente in siberia, vettore è Ixodes persulcatus;
Il capside virale è composto di tre proteine strutturali :
- proteine di rivestimento E
- proteina del core C
- proteina di membrana
La glicoproteina E svolge un ruolo centrale nella biologia delle infezioni ed è responsabile del legame e della penetrazione nella cellula bersaglio.
Altri virus assimilabili trasmessi da zecche sono:
- Omsk haemorrhagic fever virus,
- Kyasanur forest disease virus,
- Alkhurma virus,
- Langat virus.
Vettori
Le zecche vettore appartengono tipicamente a generi della famiglia Ixodidae (zecche dure):
- Ixodes spp.
- Dermacentor spp.
- Haemaphysalis spp.
Le zecche oltre che vettori sono anche serbatoi di riserva del virus in grado di garantirne la persistenza nell’ambiente oltre il periodo di attività della zecca tramite la trasmissione transovarica (l'infezione si trasmette attraverso le uova dalla madre alla prole), transtadiale (da larva a ninfe e / o da ninfe ad adulto), per co-feeding (zecca che effettua il pasto di sangue accanto ad un’altra infetta)i . L'uomo è il principale ospite terminale insieme a piccoli animali selvatici, per lo più roditori, che sono ospiti comuni.[3][4]
I piccoli mammiferi come i roditori sono ospiti e danno una virus amplificazione per il loro alto tasso riproduttivo. Gli esseri umani sono infettati sporadicamente, sia da una puntura di zecca o per l'ingestione di latte non pastorizzato o suoi prodotti lattiero-caseari.[5][6][7][8][9] Altri mammiferi (ad esempio ruminanti) possono anche essere infettati, ma il più delle volte non mostrano segni clinici.[10]
Clinica
I virus provocano encefaliti, con una fase iniziale con febbre, mal di testa e mialgia. Nei casi più gravi segue dopo circa una settimana dalla apparente guarigione clinica una seconda fase della malattia con meningoencefalite o mielite. Questa ultima tende a causare paralisi flaccida dell'arto superiore e della spalla dei muscoli respiratori. Il coinvolgimento bulbare (tronco cerebrale) porta ad insufficienza respiratoria e quindi la morte.[3] Si ritrova nel liquido cerebrospinale la presenza di neutrofili, con una leucocitosi periferica indicativo di meningite.[3]
Note
- ^ Gould EA, Solomon T, Pathogenic flaviviruses, in Lancet, vol. 371, n. 9611, 2008, pp. 500-9, DOI:10.1016/S0140-6736(08)60238-X, PMID 18262042.
- ^ Lindquist L, Vapalahti O, Tick-borne encephalitis, in Lancet, vol. 371, n. 9627, 2008, pp. 1861-71, DOI:10.1016/S0140-6736(08)60800-4, PMID 18514730.
- ^ a b c Solomon T, Mallewa M, Dengue and other emerging flaviviruses, in J. Infect., vol. 42, n. 2, 2001, pp. 104-15, DOI:10.1053/jinf.2001.0802, PMID 11531316.
- ^ (EN) Transmission | Tick-borne Encephalitis (TBE) | CDC, su www.cdc.gov. URL consultato il 14 luglio 2018.
- ^ (EN) Neda Hudopisk, Miša Korva e Evgen Janet, Tick-borne Encephalitis Associated with Consumption of Raw Goat Milk, Slovenia, 2012, in Emerging Infectious Diseases, vol. 19, n. 5, 2013-05, DOI:10.3201/eid1905.121442. URL consultato il 14 luglio 2018.
- ^ Heidemarie Holzmann, Stephan W. Aberle e Karin Stiasny, Tick-borne encephalitis from eating goat cheese in a mountain region of Austria, in Emerging Infectious Diseases, vol. 15, n. 10, 2009-10, pp. 1671-1673, DOI:10.3201/eid1510.090743. URL consultato il 14 luglio 2018.
- ^ Danielle K. Offerdahl, Niall G. Clancy e Marshall E. Bloom, Stability of a Tick-Borne Flavivirus in Milk, in Frontiers in Bioengineering and Biotechnology, vol. 4, 11 maggio 2016, DOI:10.3389/fbioe.2016.00040. URL consultato il 14 luglio 2018.
- ^ Brockmann SO, Oehme R, Buckenmaier T, Beer M, Jeffery-Smith A, Spannenkrebs M, Haag-Milz S, Wagner-Wiening C, Schlegel C, Fritz J, Zange S, Bestehorn M, Lindau A, Hoffmann D, Tiberi S, Mackenstedt U, Dobler G, A cluster of two human cases of tick-borne encephalitis (TBE) transmitted by unpasteurised goat milk and cheese in Germany, May 2016, in Euro Surveill., vol. 23, n. 15, April 2018, DOI:10.2807/1560-7917.ES.2018.23.15.17-00336, PMC 6836198, PMID 29667575.
- ^ Markovinović L, Kosanović Ličina ML, Tešić V, Vojvodić D, Vladušić Lucić I, Kniewald T, Vukas T, Kutleša M, Krajinović LC, An outbreak of tick-borne encephalitis associated with raw goat milk and cheese consumption, Croatia, 2015, in Infection, vol. 44, n. 5, October 2016, pp. 661-5, DOI:10.1007/s15010-016-0917-8, PMID 27364148.
- ^ Valarcher JF, Hägglund S, Juremalm M, Blomqvist G, Renström L, Zohari S, Leijon M, Chirico J, Tick-borne encephalitis, in Rev. - Off. Int. Epizoot., vol. 34, n. 2, 2015, pp. 453-66, PMID 26601448.
Bibliografia
Testi
- Pei-Yong Shi, Molecular Virology and Control of Flaviviruses, Horizon Scientific Press, 1º gennaio 2012, ISBN 978-1-904455-92-9.
- Paul Shapshak, John T. Sinnott, Charurut Somboonwit and Jens Kuhn, Global Virology I - Identifying and Investigating Viral Diseases, Springer, 13 luglio 2015, pp. 487–, ISBN 978-1-4939-2410-3.
- Richard A. Kaslow, Lawrence R. Stanberry and James W. Le Duc, Viral Infections of Humans: Epidemiology and Control, Springer, 27 settembre 2014, pp. 405–, ISBN 978-1-4899-7448-8.
- Dongyou Liu, Molecular Detection of Human Viral Pathogens, CRC Press, 23 novembre 2010, pp. 314–, ISBN 978-1-4398-1237-2.
- Flavivirus Infections—Advances in Research and Treatment: 2012 Edition: ScholarlyBrief, ScholarlyEditions, 26 dicembre 2012, pp. 6–, ISBN 978-1-4816-1346-0.
- Walter R Schlesinge, The Togaviruses: bio,struc,replication, Elsevier, 2 dicembre 2012, pp. 675–, ISBN 978-0-323-13826-0.
- and Subhash Vasudevan Duane J. Gubler, Eng Eong Ooi, Jeremy Farrar, Dengue and Dengue Hemorrhagic Fever, 2nd Edition, CABI, 29 agosto 2014, pp. 322–, ISBN 978-1-84593-964-9.
- Arbovirus Encephalitis—Advances in Research and Treatment: 2013 Edition: ScholarlyBrief, ScholarlyEditions, 21 giugno 2013, pp. 46–, ISBN 978-1-4816-8522-1.
- Japanese Encephalitis: New Insights for the Healthcare Professional: 2013 Edition: ScholarlyPaper, ScholarlyEditions, 22 luglio 2013, pp. 26–, ISBN 978-1-4816-5982-6.
- Michael W. Scheld, Christina M. Marra and Richard J. Whitley, Infections of the Central Nervous System, Lippincott Williams & Wilkins, 2014, pp. 210–, ISBN 978-1-4511-7372-7.
- Charles H. Calisher & Diane E. Griffin, Emergence and Control of Zoonotic Viral Encephalitides, Springer Science & Business Media, 23 marzo 2004, pp. 191–, ISBN 978-3-211-20454-2.
- Erik De Clercq, Earl R. Kern, Handbook of Viral Bioterrorism and Biodefense, Elsevier, 2003, pp. 129–, ISBN 978-0-444-51326-7.
- Richard V. Goering, Cedric A. Mims, Hazel Dockrell & Mark Zuckerman, Ivan M. Roitt, Peter L. Chiodini, Mims' Medical Microbiology,With STUDENT CONSULT Online Access ,5: Mims' Medical Microbiology, Elsevier Health Sciences, 2013, pp. 370–, ISBN 0-7234-3601-0.
- Debra C. Sellon & Maureen Long, Equine Infectious Diseases, Elsevier Health Sciences, 8 dicembre 2006, pp. 198–, ISBN 1-4377-1061-1.
- Karl Maramorosch & Frederick A. Murphy, Advances in Virus Research, Elsevier Science, 18 aprile 2014, ISBN 978-0-12-800400-5.
Riviste
- Takamatsu K, Kishino W, Suehiro T, Yamano T, Ohno F, Plasma apolipoprotein H (beta 2-glycoprotein I) phenotype frequencies in a Japanese population, in Jinrui Idengaku Zasshi, vol. 34, n. 4, 1989, pp. 279-83, DOI:10.1007/BF01929209, PMID 2634788.
- Klema VJ, Padmanabhan R, Choi KH, Flaviviral Replication Complex: Coordination between RNA Synthesis and 51-RNA Capping, in Viruses, vol. 7, n. 8, 2015, pp. 4640-56, DOI:10.3390/v7082837, PMC 4576198, PMID 26287232.
- Jeffries CL, Walker T, The Potential Use of Wolbachia-Based Mosquito Biocontrol Strategies for Japanese Encephalitis, in PLoS Negl Trop Dis, vol. 9, n. 6, 2015, pp. e0003576, DOI:10.1371/journal.pntd.0003576, PMC 4472807, PMID 26086337.
- Wu J, Liu W, Gong P, A Structural Overview of RNA-Dependent RNA Polymerases from the Flaviviridae Family, in Int J Mol Sci, vol. 16, n. 6, 2015, pp. 12943-57, DOI:10.3390/ijms160612943, PMC 4490480, PMID 26062131.
- Blitvich BJ, Firth AE, Insect-specific flaviviruses: a systematic review of their discovery, host range, mode of transmission, superinfection exclusion potential and genomic organization, in Viruses, vol. 7, n. 4, 2015, pp. 1927-59, DOI:10.3390/v7041927, PMC 4411683, PMID 25866904.
- Mezochow AK, Henry R, Blumberg EA, Kotton CN, Transfusion transmitted infections in solid organ transplantation, in Am. J. Transplant., vol. 15, n. 2, 2015, pp. 547-54, DOI:10.1111/ajt.13006, PMID 25612502.
- Das P, Infectious disease surveillance update, in Lancet Infect Dis, vol. 4, n. 8, 2004, p. 481, PMID 15298027.
- Blitvich BJ, Firth AE, Insect-specific flaviviruses: a systematic review of their discovery, host range, mode of transmission, superinfection exclusion potential and genomic organization, in Viruses, vol. 7, n. 4, 2015, pp. 1927-59, DOI:10.3390/v7041927, PMC 4411683, PMID 25866904.
- Qin XC, Shi M, Tian JH, Lin XD, Gao DY, He JR, Wang JB, Li CX, Kang YJ, Yu B, Zhou DJ, Xu J, Plyusnin A, Holmes EC, Zhang YZ, A tick-borne segmented RNA virus contains genome segments derived from unsegmented viral ancestors, in Proc. Natl. Acad. Sci. U.S.A., vol. 111, n. 18, 2014, pp. 6744-9, DOI:10.1073/pnas.1324194111, PMC 4020047, PMID 24753611.
- Brecher M, Zhang J, Li H, The flavivirus protease as a target for drug discovery, in Virol Sin, vol. 28, n. 6, 2013, pp. 326-36, DOI:10.1007/s12250-013-3390-x, PMC 3927373, PMID 24242363.
- Bollati M, Alvarez K, Assenberg R, Baronti C, Canard B, Cook S, Coutard B, Decroly E, de Lamballerie X, Gould EA, Grard G, Grimes JM, Hilgenfeld R, Jansson AM, Malet H, Mancini EJ, Mastrangelo E, Mattevi A, Milani M, Moureau G, Neyts J, Owens RJ, Ren J, Selisko B, Speroni S, Steuber H, Stuart DI, Unge T, Bolognesi M, Structure and functionality in flavivirus NS-proteins: perspectives for drug design, in Antiviral Res., vol. 87, n. 2, 2010, pp. 125-48, DOI:10.1016/j.antiviral.2009.11.009, PMC 3918146, PMID 19945487.
- Wu J, Bera AK, Kuhn RJ, Smith JL, Structure of the Flavivirus helicase: implications for catalytic activity, protein interactions, and proteolytic processing, in J. Virol., vol. 79, n. 16, 2005, pp. 10268-77, DOI:10.1128/JVI.79.16.10268-10277.2005, PMC 1182653, PMID 16051820.
- Kuno G, Chang GJ, Tsuchiya KR, Karabatsos N, Cropp CB, Phylogeny of the genus Flavivirus, in J. Virol., vol. 72, n. 1, 1998, pp. 73-83, PMC 109351, PMID 9420202.
- Zanotto PM, Ernest A. Gould, George F. Gao, Paul H. Harvey e Edward C. Holmes, Population dynamics of flaviviruses revealed by molecular phylogenies, in Proc Natl Acad Sci U S A., vol. 93, n. 2, Jan 1996, pp. 548-53, Bibcode:1996PNAS...93..548Z, DOI:10.1073/pnas.93.2.548, PMC 40088, PMID 8570593.
- Murray CL, Jones CT, Rice CM, Architects of assembly: roles of Flaviviridae non-structural proteins in virion morphogenesis, in Nat. Rev. Microbiol., vol. 6, n. 9, 2008, pp. 699-708, DOI:10.1038/nrmicro1928, PMC 2764292, PMID 18587411.
Voci correlate
Altri progetti
Altri progetti
- Wikimedia Commons
- Wikispecies
 Wikimedia Commons contiene immagini o altri file su Flavivirus della encefalite trasmessa da zecche
Wikimedia Commons contiene immagini o altri file su Flavivirus della encefalite trasmessa da zecche Wikispecies contiene informazioni su Flavivirus della encefalite trasmessa da zecche
Wikispecies contiene informazioni su Flavivirus della encefalite trasmessa da zecche
Collegamenti esterni
- (EN) MicrobiologyBytes: Flavivirus, su microbiologybytes.com. URL consultato il 17 gennaio 2016 (archiviato dall'url originale il 23 aprile 2015).
- (EN) Viralzone: Flavivirus, su expasy.org. URL consultato il 16 gennaio 2016.
- (EN) Virus Pathogen Database and Analysis Resource (ViPR) - Flaviviridae - Genome database with visualization and analysis tools, su viprbrc.org. URL consultato il 9 febbraio 2016.
V · D · M | |||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Tipo di virus |
| ||||||||||||||||||||||
| DNA |
| ||||||||||||||||||||||
| RNA |
| ||||||||||||||||||||||
| RT |
| ||||||||||||||||||||||
| Viroidi |
| ||||||||||||||||||||||
| Virus · Classificazione dei virus · Classificazione di Baltimore | |||||||||||||||||||||||
V · D · M | ||
|---|---|---|
| Componenti virali | Capside · Capsomero · Pericapside · Peplomero |  |
| Replicazione virale | Ciclo litico e lisogeno · Provirus · Profago · Virione | |
| Classificazione dei virus | Classificazione di Baltimore · International Committee on Taxonomy of Viruses · Teoria delle quasispecie | |
| Clinica | Malattie infettive virali · Viremia · Titolazione virale · Antivirale · Oncovirus | |
| Organismi parassitati | Viroma umano · Medicina · Medicina veterinaria · Fitovirus · Micovirus · Batteriofagi · Virofagi | |
 Portale Microbiologia: accedi alle voci di Wikipedia che trattano di microbiologia
Portale Microbiologia: accedi alle voci di Wikipedia che trattano di microbiologia











