Riarrangiamento di Carroll
Il riarrangiamento di Carroll è una reazione di riarrangiamento in chimica organica e comporta la trasformazione di un estere β-cheto allile ad acido α-allil-β-chetocarbossilico.[1]
Questa reazione organica è accompagnata da decarbossilazione dando come prodotto finale un γ,δ-allilchetone. Il riarrangiamento di Carroll è un adattamento del riarrangiamento di Claisen e di un'allilazione decarbossilativa.
Meccanismo di reazione
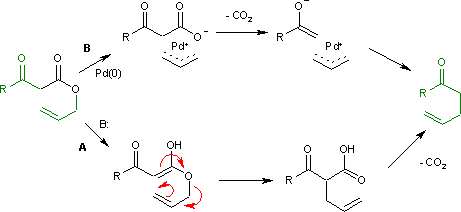
La reazione di Carroll (1940) avviene in presenza di una base e ad alta temperatura di reazione (step A) attraverso un enolo intermedio che subisce un riarrangiamento di Claisen elettrociclico. Lo stadio successivo è una decarbossilazione. Con il palladio(0) come catalizzatore, la reazione (Tsuji, 1980) è più blanda (step B) con un catione allile intermedio / complesso organometallico dell'anione acido carbossilico.[2]
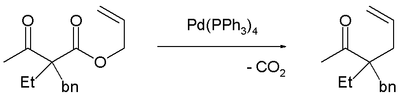
La decarbossilazione precede l'allilazione come evidenziato da questa reazione catalizzata dal tetracis(trifenilfosfina)palladio(0):[3]
Allilazione decarbossilativa asimmetrica
Con l'introduzione di ligandi chirali adatti, la reazione diventa enantioselettiva.[4]
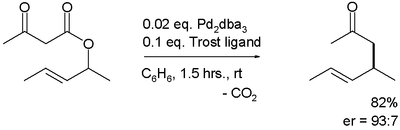
Il primo riarrangiamento asimmetrico in letteratura è stato catalizzato da tris(dibenzilideneacetone)dipalladio(0) e dal ligande di Trost:[3]
Una reazione simile[5] usa anche naftolo per catalizzare.

Questa reazione produce un enantiomero con ee dell'88%. Resta da vedere se questa reazione avrà un'ampia portata perché il gruppo acetamido sembra essere un prerequisito importante.
Con lo stesso catalizzatore ma un ligando diverso si ottiene un riarrangiamento asimmetrico con una reazione enantioconvergente:[6]
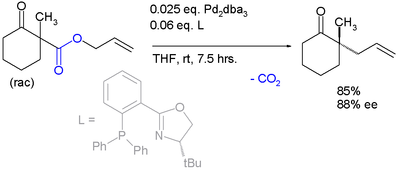
L'ambito di applicazione è esteso all'α-alchilazione asimmetrica dei chetoni mascherati dai loro enol esteri di carbonato:[7]

Note
- ^ (EN) Carroll, M. F., 131. Addition of α,β-unsaturated alcohols to the active methylene group. Part I. The action of ethyl acetoacetate on linalool and geraniol, in J. Chem. Soc., 1940, pp. 704-706, DOI:10.1039/JR9400000704.
- ^ (EN) Isao Shimizu, Toshiro Yamada, Jiro Tsuji, Palladium-catalyzed rearrangement of allylic esters of acetoacetic acid to give γ,δ-unsaturated methyl ketones, in Tetrahedron Lett., vol. 21, n. 33, 1980, pp. 3199-3202, DOI:10.1016/S0040-4039(00)77444-2.
- ^ a b (EN) Erin C. Burger; Jon A. Tunge, Asymmetric Allylic Alkylation of Ketone Enolates: An Asymmetric Claisen Surrogate, in Org. Lett., vol. 6, n. 22, 2004, pp. 4113-4115, DOI:10.1021/ol048149t.
- ^ (EN) Shu-Li You; Li-Xin Dai, Enantioselective Palladium-Catalyzed Decarboxylative Allylic Alkylations, in Angew. Chem. Int. Ed., vol. 45, 2006, pp. 5246-5248, DOI:10.1002/anie.200601889.
- ^ (EN) Kuwano, R.; Ishida N.; Murakami, M., Asymmetric Carroll rearrangement of allyl α-acetamido-β-ketocarboxylates catalysed by a chiral palladium complex, in Chem. Commun., n. 31, 2005, pp. 3951-3952, DOI:10.1039/b505105c.
- ^ (EN) Justin T. Mohr; Douglas C. Behenna; Andrew M. Harned; Brian M. Stoltz, Deracemization of Quaternary Stereocenters by Pd-Catalyzed Enantioconvergent Decarboxylative Allylation of Racemic b-Ketoesters, in Angew. Chem. Int. Ed., vol. 44, 2005, pp. 6924-6927, DOI:10.1002/anie.200502018.
- ^ (EN) Barry M. Trost, Jiayi Xu, Palladium-Catalyzed Asymmetric Allylic α-Alkylation of Acyclic Ketones, in J. Am. Chem. Soc., vol. 127, n. 49, 2005, pp. 17180-17181, DOI:10.1021/ja055968f.
Voci correlate
Altri progetti
Altri progetti
- Wikimedia Commons
 Wikimedia Commons contiene immagini o altri file su Riarrangiamento di Carroll
Wikimedia Commons contiene immagini o altri file su Riarrangiamento di Carroll
 Portale Chimica: il portale della scienza della composizione, delle proprietà e delle trasformazioni della materia
Portale Chimica: il portale della scienza della composizione, delle proprietà e delle trasformazioni della materia










