Trichlorosilane
| Trichlorosilane | |||
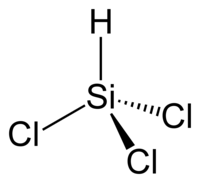   | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | trichlorosilane | ||
| No CAS | 10025-78-2 | ||
| No ECHA | 100.030.026 | ||
| No CE | 233-042-5 | ||
| No RTECS | VV5950000 | ||
| PubChem | 24811 | ||
| SMILES | [SiH](Cl)(Cl)Cl PubChem, vue 3D | ||
| InChI | InChI : vue 3D InChI=1S/Cl3HSi/c1-4(2)3/h4H InChIKey : ZDHXKXAHOVTTAH-UHFFFAOYSA-N | ||
| Apparence | liquide incolore à l'odeur âcre, aigre[1] | ||
| Propriétés chimiques | |||
| Formule | HCl3SiSiHCl3 | ||
| Masse molaire[2] | 135,452 ± 0,006 g/mol H 0,74 %, Cl 78,52 %, Si 20,73 %, | ||
| Propriétés physiques | |||
| T° fusion | −134 °C[1] | ||
| T° ébullition | 32-34 °C[3],[1] | ||
| Solubilité | décomp. dans l'eau | ||
| T° d'auto-inflammation | 195 °C[1] | ||
| Point d’éclair | −51 °C[3] −20 °C[1] | ||
| Limites d’explosivité dans l’air | min 6,9 vol. % soit 385 g·m-3[1] | ||
| Pression de vapeur saturante | 9,75 psi à 20 °C[3] 660 mbar à 20 °C[1] 951 mbar à 30 °C[1] | ||
| Précautions | |||
| SGH[3],[1] | |||
   H224 : Liquide et vapeurs extrêmement inflammables H250 : S'enflamme spontanément au contact de l'air H302 : Nocif en cas d'ingestion H314 : Provoque de graves brûlures de la peau et des lésions oculaires H332 : Nocif par inhalation P210 : Tenir à l’écart de la chaleur/des étincelles/des flammes nues/des surfaces chaudes. — Ne pas fumer. P222 : Ne pas laisser au contact de l’air. P231 : Manipuler sous gaz inerte. P280 : Porter des gants de protection/des vêtements de protection/un équipement de protection des yeux/du visage. P305+P351+P338 : En cas de contact avec les yeux : rincer avec précaution à l’eau pendant plusieurs minutes. Enlever les lentilles de contact si la victime en porte et si elles peuvent être facilement enlevées. Continuer à rincer. P422 : Stocker le contenu sous … | |||
| Transport[1] | |||
Numéro ONU : 1295 : TRICHLOROSILANE Classe : 4.3 Code de classification : Code non reconnu : X338. Signaler une erreur : Discussion_Modèle:ADR Étiquette :  4.3 : Matières qui, au contact de l'eau, dégagent des gaz inflammables Emballage : Groupe d'emballage I : matières très dangereuses ; | |||
| Unités du SI et CNTP, sauf indication contraire. | |||
modifier  | |||
Le trichlorosilane est un composé chimique contenant du silicium, de l'hydrogène et du chlore. À des températures élevées, il se décompose pour produire du silicium. Le trichlorosilane purifié est la principale source de silicium ultra-pur dans l'industrie des semi-conducteurs. Dans l'eau, il se décompose rapidement pour produire un polymère de silicone tout en donnant de l'acide chlorhydrique. En raison de sa réactivité et une grande disponibilité, il est fréquemment utilisé dans la synthèse de composés contenant du silicium organique.
Production
Industriellement, le trichlorosilane est produit en soufflant du chlorure d'hydrogène sur un lit de poudre de silicium à 300 °C. Les deux composés réagissent pour former du trichlorosilane et de l'hydrogène suivant l'équation chimique :
- Si + 3 HCl → HSiCl3 + H2.
Un réacteur bien conçu peut atteindre un rendement de 80-90 % de trichlorosilane. Les sous-produits principaux sont le tétrachlorure de silicium (SiCl4), hexachlorodisilane (Si2Cl6) et le dichlorosilane (H2SiCl2), desquels le trichlorosilane peut être séparé par distillation.
Le processus inverse est utilisé pour la production de silicium plus pur.
Notes et références
- ↑ a b c d e f g h i j et k Entrée « Trichlorosilane » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 19 mars 2012 (JavaScript nécessaire)
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ a b c d et e Fiche Sigma-Aldrich du composé Trichlorosilane, consultée le 19 mars 2012.
v · m Halogénosilanes | |
|---|---|
| Fluore | |
| Chlore |
|
| Brome |
|
| Iode |
|
 Portail de la chimie
Portail de la chimie










