| PPID |
|---|
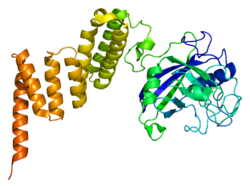 |
|
| Identifiants |
|---|
| Aliases | PPID, Cyclophiline D |
|---|
| IDs externes | OMIM: 601753 MGI: 1914988 HomoloGene: 31283 GeneCards: PPID |
|---|
| Position du gène (Homme) |
|---|
 | | Chr. | Chromosome 4 humain[1] |
|---|
| | Locus | 4q32.1 | Début | 158,709,127 bp[1] |
|---|
| Fin | 158,723,396 bp[1] |
|---|
|
| Position du gène (Souris) |
|---|
 | | Chr. | Chromosome 3 (souris)[2] |
|---|
| | Locus | 3|3 E3 | Début | 79,498,649 bp[2] |
|---|
| Fin | 79,510,957 bp[2] |
|---|
|
| Expression génétique |
|---|
| Bgee | | Humain | Souris (orthologue) |
|---|
| Fortement exprimé dans | - right lobe of liver
- muscle de la cuisse
- muscle gastrocnémien
- mucosa of transverse colon
- gonade
- Skeletal muscle tissue of rectus abdominis
- right adrenal cortex
- rectum
- body of tongue
- ventricule gauche
|
| | Fortement exprimé dans | - tail of embryo
- Épiblaste
- gyrus cingulaire
- embryon
- embryon
- tubercule génital
- tube neural
- ventricular zone
- amygdale
- otic vesicle
|
| | Plus de données d'expression de référence |
|
|---|
| BioGPS | 
 | | Plus de données d'expression de référence |
|
|---|
|
| Gene Ontology |
|---|
| Fonction moléculaire | - Hsp90 protein binding
- heat shock protein binding
- transcription factor binding
- isomerase activity
- peptidyl-prolyl cis-trans isomerase activity
- Hsp70 protein binding
- liaison protéique
- estrogen receptor binding
- cyclosporin A binding
- unfolded protein binding
| | Composant cellulaire | - cytoplasme
- nucléole
- noyau
- cytosol
- nucléoplasme
- mitochondrie
| | Processus biologique | - chaperone-mediated protein folding
- cellular response to UV-A
- excrétion virale
- lipid droplet organization
- negative regulation of transcription by RNA polymerase II
- repliement de protéine
- positive regulation of protein secretion
- positive regulation of apoptotic process
- protein transport
- positive regulation of viral genome replication
- apoptose
- protein-containing complex assembly
- protein peptidyl-prolyl isomerization
- protein refolding
- negative regulation of apoptotic process
- regulation of mitochondrial membrane potential
| | Sources:Amigo / QuickGO |
|
| Orthologues |
|---|
| Espèces | Homme | Souris |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (mRNA) | | |
|---|
| RefSeq (protéine) | | |
|---|
| Localisation (UCSC) | Chr 4: 158.71 – 158.72 Mb | Chr 3: 79.5 – 79.51 Mb |
|---|
| Publication PubMed | [3] | [4] |
|---|
|
| Wikidata |
| Voir/Editer Humain | Voir/Editer Souris |
|
La cyclophiline D est une protéine appartenant à la famille des cyclophilines ayant une activité de Peptidyl prolyl isomérase. Son gène est le PPID situé sur le chromosome 4 humain.
Rôles
Comme les autres peptidyl prolyl isomérases, elle permet la transformation de certaines protéines de la forme trans à la forme cis, modulant leur activité.
Elle est exprimée dans toutes les cellules humaines[5] au niveau des mitochondries où elle permet de réguler la perméabilité des pores de la paroi[6]. Elle intervient également dans la régulation du cycle de Krebs, dans la dégradation des protéines et dans le métabolisme du pyruvate[7].
L'inhibition de la cyclophiline D pourrait être une cible pour le traitement de la maladie d'Alzheimer[8] ou de la maladie de Parkinson[9].
Notes et références
- ↑ a b et c GRCh38: Ensembl release 89: ENSG00000171497 - Ensembl, May 2017
- ↑ a b et c GRCm38: Ensembl release 89: ENSMUSG00000027804 - Ensembl, May 2017
- ↑ « Publications PubMed pour l'Homme », sur National Center for Biotechnology Information, U.S. National Library of Medicine
- ↑ « Publications PubMed pour la Souris », sur National Center for Biotechnology Information, U.S. National Library of Medicine
- ↑ (en) Perrucci GL, Gowran A, Zanobini M et al. « Peptidyl-prolyl isomerases: a full cast of critical actors in cardiovascular diseases » Cardiovasc Res. 2015;106:353-364
- ↑ Elrod JW, Wong R, Mishra S et al. Cyclophilin D controls mitochondrial pore-dependent Ca(2+) exchange, metabolic flexibility, and propensity for heart failure in mice, J Clin Invest, 2010;120:3680–3687
- ↑ Menazza S, Wong R, Nguyen T, Wang G, Gucek M, Murphy E, CypD(-/-) hearts have altered levels of proteins involved in Krebs cycle, branch chain amino acid degradation and pyruvate metabolism, J Mol Cell Cardiol, 2013;56:81–90
- ↑ Du H, Guo L, Fang F et al. Cyclophilin D deficiency attenuates mitochondrial and neuronal perturbation and ameliorates learning and memory in Alzheimer's disease, Nat Med, 2008;14:1097–1105
- ↑ Forte M, Gold BG, Marracci G et al. Cyclophilin D inactivation protects axons in experimental autoimmune encephalomyelitis, an animal model of multiple sclerosis, Proc Natl Acad Sci USA, 2007;104:7558–7563
 Portail de la biologie cellulaire et moléculaire
Portail de la biologie cellulaire et moléculaire  Portail de la médecine
Portail de la médecine
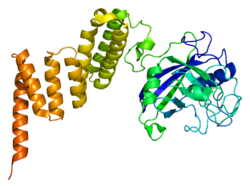
 Portail de la biologie cellulaire et moléculaire
Portail de la biologie cellulaire et moléculaire  Portail de la médecine
Portail de la médecine 

















