Azoture de méthyle
| Azoture de méthyle | |
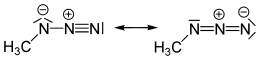 Mésomères de l'azoture de méthyle. | |
| Identification | |
|---|---|
| Nom UICPA | azidométhane |
| Synonymes | méthylazoture |
| No CAS | 624-90-8 |
| PubChem | 79079 |
| SMILES | CN=[N+]=[N-] PubChem, vue 3D |
| InChI | Std. InChI : vue 3D InChI=1S/CH3N3/c1-3-4-2/h1H3 Std. InChIKey : PBTHJVDBCFJQGG-UHFFFAOYSA-N |
| Propriétés chimiques | |
| Formule | CH3N3 [Isomères] |
| Masse molaire[1] | 57,054 6 ± 0,001 6 g/mol C 21,05 %, H 5,3 %, N 73,65 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
modifier  | |
L'azoture de méthane est un composé chimique de formule CH3–N=N+=N−, en résonance avec la structure CH3–N−–N+≡N[2]. Il s'agit d'un explosif, qui se décompose selon la réaction[3] :
- CH3N3 → CH2NH + N2.
Il pourrait être impliqué dans la chimie prébiotique sur des grains de poussière interstellaire sous l'effet de rayons cosmiques et de photons énergétiques[4].
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ (en) Linus Pauling et L. O. Brockway, « The Adjacent Charge Rule and the Structure of Methyl Azide, Methyl Nitrate, and Fluorine Nitrate », Journal of the American Chemical Society, vol. 59, no 1, , p. 13-20 (lire en ligne) DOI 10.1021/ja01280a005
- ↑ (en) M. S. O'Dell Jr. et B. Darwent, « Thermal decomposition of methyl azide », Revue canadienne de chimie, vol. 48, no 7, , p. 1140-1147 DOI 10.1139/v70-187
- ↑ (en) Alfredo Quinto-Hernandez, Alec M. Wodtke, Chris J. Bennett, Y. Seol Kim et Ralf I. Kaiser, « On the Interaction of Methyl Azide (CH3N3) Ices with Ionizing Radiation: Formation of Methanimine (CH2NH), Hydrogen Cyanide (HCN), and Hydrogen Isocyanide (HNC) », Journal of Physical Chemistry, vol. 115, no 3, , p. 250-264 (DOI 10.1021/jp103028v, lire en ligne)
 Portail de la chimie
Portail de la chimie











