Bromoacetona
 Estructura química | ||
 Estructura 3D | ||
| Nombre IUPAC | ||
| 1-Bromoacetona | ||
| General | ||
| Otros nombres | 1-Bromo-2-propanona; α-Bromoacetona; Monobromoacetona | |
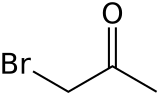
| Fórmula molecular | CH3COCH2Br | |
| Identificadores | ||
| Número CAS | 598-31-2[1] | |
| Número RTECS | UC0525000 | |
| ChEBI | 51845 | |
| ChEMBL | CHEMBL1085947 | |
| InChI InChI=InChI=1S/C3H5BrO/c1-3(5)2-4/h2H2,1H3 Key: VQFAIAKCILWQPZ-UHFFFAOYSA-N | ||
| Propiedades físicas | ||
| Apariencia | Líquido incoloro | |
| Punto de fusión | −36,5 °C (237 K) | |
| Punto de ebullición | 137 °C (410 K) | |
| Presión de vapor | 1.1 kPa (20 °C) | |
| Peligrosidad | ||
| SGA |   | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
[editar datos en Wikidata] | ||
La bromoacetona es un compuesto orgánico con la fórmula CH3COCH2Br. Este líquido incoloro es un agente lacrimógeno, precursor de otros compuestos orgánicos.
Origen
Es una sustancia presente de forma natural (menos de 1%) en el aceite esencial de un alga que se encuentra en las proximidades de las islas Hawái.[2]
Síntesis
Está disponible comercialmente, en ocasiones estabilizada con óxido de magnesio. Fue descripta por primera vez en el siglo XIX, trabajo que se le atribuye a N. Sokolowsky.[3]

La bromacetona se prepara mediante la combinación de bromo y acetona,[4] con un ácido catalítico. Si se utiliza una base, el producto obtenido será bromoformo:
- CH3C (O) CH3 + Br2 → CH3C (O) CH2Br + HBr
La principal dificultad con este método es el exceso de bromación, que resulta en productos di y tribrominados. En términos de mecanismo, como con todas las cetonas, la acetona se enoliza en presencia de ácidos o bases. El carbono alfa a continuación, se somete a sustitución electrófila con bromo.[5]
Aplicaciones
Fue utilizada en la Primera Guerra Mundial como arma química, llamada BA por británicos y B-Stoff (cruz blanca) por los alemanes. Debido a su toxicidad, es obsoleta como un agente de control de disturbios y ya no se utiliza. Es además un reactivo versátil en la síntesis orgánica, por ejemplo como precursor en la reacción de producción de hidroxiacetona (N º CAS 116-09-6).[6]
Véase también
Referencias
- ↑ Número CAS
- ↑ Burreson, B. J.; Moore, R. E.; Roller, P. P. (1976). «Volatile halogen compounds in the alga Asparagopsis taxiformis (Rhodophyta)». Journal of Agricultural and Food Chemistry 24 (4): 856-861. doi:10.1021/jf60206a040.
- ↑ Wagner, G. (1876). «Sitzung der russischen chemischen Gesellschaft am 7./19. October 1876». Berichte der Deutschen Chemischen Gesellschaft 9 (2): 1687-1688. doi:10.1002/cber.187600902196.
- ↑ Levene, P. A. (1930). "Bromoacetone". Org. Synth. 10: 12; Coll. Vol. 2: 88.
- ↑ Reusch, W. (5 de mayo de 2013). «Carbonyl Reactivity». Virtual Textbook of Organic Chemistry. Michigan State University. Archivado desde el original el 21 de junio de 2010. Consultado el 4 de julio de 2014.
- ↑ Levene, P. A.; Walti, A. (1930). "Acetol". Org. Synth. 10: 1; Coll. Vol. 2: 5.
Enlaces externos
- Esta obra contiene una traducción parcial derivada de «Bromoacetone» de Wikipedia en inglés, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.
 Datos: Q421365
Datos: Q421365 Multimedia: Bromoacetone / Q421365
Multimedia: Bromoacetone / Q421365












